目次
RECIST 1.1 とは
RECIST 1.1(Response Evaluation Criteria in Solid Tumors)(1)は、固形がんの悪性腫瘍薬の治療効果を判定する際に用いられる基準のひとつで、有効性を評価する臨床試験において多くの薬剤の承認に用いられています。RECIST 1.1は、CTやMRIのような画像検査をもとに、悪性腫瘍薬の投与前後で腫瘍のサイズを計測し、患者ごとに治療効果を判定します。臨床試験において、RECIST 1.1をもとに抗悪性腫瘍薬の客観的奏効率(ORR; overall response rate)や無増悪生存期間(PFS; progression-free survival)等が算出されます。
RECIST効果判定のフロー
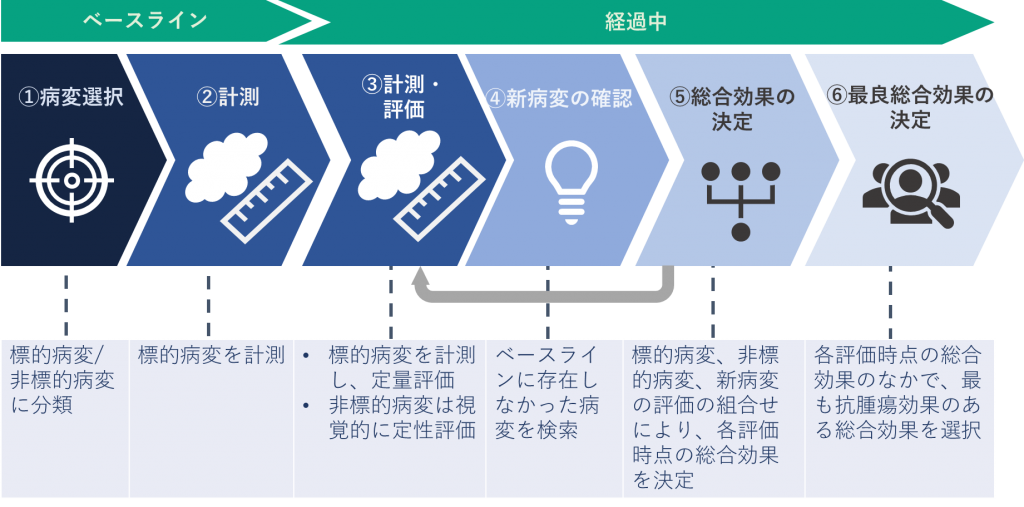
①ベースラインの病変選択
ベースラインにおいて、以下のルールに従い、病変を標的病変と非標的病変に分類します。なお、5病変を超える標的病変が認められた場合、計測の再現性が良い病変かつ径が大きい病変から優先的に選択します。

②ベースラインの計測
標的病変を計測します。非リンパ節病変は長径、リンパ節は短径を計測します。

③経過中の計測・評価
ベースラインで計測した標的病変を計測します。原則、同じ画像検査、撮像条件で計測します。
各評価時点において。標的病変、非標的病変に対し、CRやPDなどの効果を判定します。非標的病変は、腫瘍マーカー値を加えて評価します。

④新病変の確認
ベースラインに存在しなかった病変を検索します。
⑤総合効果の決定
各評価時点において、標的病変、非標的病変、新病変の組合せに従い、総合効果を決定します。各評価時点において、③計測・評価→④新病変の確認→⑤総合効果の決定を実施します。
| 標的病変 | 非標的病変 | 新病変 | 総合効果 |
|---|---|---|---|
| CR | CR | なし | CR |
| CR | Non-CR/non-PD | なし | PR |
| CR | 評価なし | なし | PR |
| PR | Non-CR/non-PD | なし | PR |
| SD | Non-CR/non-PD | なし | SD |
| 評価の欠損あり | Non-CR | なし | NE |
| PD | 問わない | ありorなし | PD |
| 問わない | CR | ありorなし | PD |
| 問わない | 問わない | あり | PD |
⑥最良総合効果の決定
すべての評価時点の総合効果を判定したあと、総合効果のなかで最も抗腫瘍効果のある最良総合効果を決定します。ひとつの評価時点の総合効果がCRまたはPRの場合、その評価時点をもって最良総合効果をCRまたはPRとすると、標的病変の測定誤差の影響に起因した評価である可能性があります。標的病変の測定誤差の影響を低減させることを目的として、客観的奏効率などの腫瘍縮小効果が主要評価項目である臨床試験において、最良総合効果をCRおよびPRとするために、2回連続した評価時点が臨床試験ごとに設定した期間(確定期間)以上である必要があります。
終わりに
RECIST 1.1は固形がんの抗悪性腫瘍薬の治療効果を判定する基準で、臨床試験において多く利用されています。
近年、RECIST 1.1のように画像検査を利用した臨床試験(Imaging study)は増加傾向にあります(詳細は「Imaging Endpointの利用状況 Imaging Endpoint List 」を参照してください)。RECIST 1.1のような効果判定基準を用いた評価を実施する場合、各施設で評価する方法と中央判定にて一元化して評価する方法があります。中央判定を実施することにより、バイアスが低減された精度の高い評価結果を算出することができます。詳細は「中央判定の方法論とImaging CROの役割:概論 」を参照してください。
参考
- Eisenhauer EA, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1). Eur J Cancer 2009; 45 (2): 228―247
